
بطاقة الوحدة:
- عنوانها: كيمياء المادة
- فصولها: تركيب الذرة – الجدول الدوري
- مادة: العلوم.
- الصف: الثاني المتوسط.
- الفصل الدراسي: الثاني.
- المدارس/المناهج: السعودية.
- الهدف: توفير إجابات للأسئلة.
الجزء الأول: أسئلة الاختيار من متعدد
اختر رمز الإجابة الصحيحة فيما يأتي:
1. أي مما يأتي لا يعد عنصرًا:
- أ. الحديد.
- ب. الفولاذ.
- ج. الكربون.
- د. الأكسجين.
استخدم الرسم البياني التالي للإجابة عن السؤالين 2، 3:
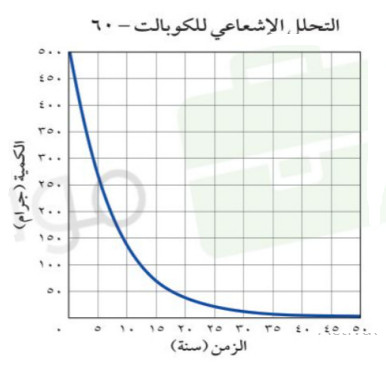
2. يظهر الرسم البياني السابق التحلل الإشعاعي لكمية مقدارها 500 جم من الكوبالت -60، ما عمر النصف له؟
- أ. 5,27 سنوات.
- ب. 21,08 سنة.
- ج. 10,54 سنوات.
- د. 0. 60 سنة.
3. كم يتبقى من الكوبالت -60 بعد 20 عاما؟
- أ. 30 جم.
- ب. 90 جم.
- ج. 60 جم.
- د. 120جم.
استعن بالجدول الآتي للإجابة عن السؤالين 4 و 5.
| نظائر النيتروجين | ||
| النظير | العدد الكتلي | عدد البروتونات |
| نيتروجين -12 | 12 | 7 |
| نيتروجين -13 | 13 | 7 |
| نيتروجين- 14 | 14 | 7 |
| نيتروجين -15 | 15 | 7 |
4. يظهر الجدول السابق خصائص بعض نظائر النيتروجين. ما عدد النيوترونات في نظير النيتروجين -15؟
- أ. 7
- ب. 14
- ج. 8
- د. 15
5. أي نظير من النظائر السابقة أقل استقرارًا؟
- أ. النيتروجين -15.
- ب. النيتروجين-13.
- ج. النيتروجين-14.
- د. النيتروجين-12.
6. أي مما يأتي أصغر كتلة؟
- أ. الإلكترون.
- ب. البروتون.
- ج. النواة.
- د. النيوترون.
7. أي العناصر الآتية الأثقل وهو في الحالة الطبيعية؟
- أ. Ac.
- ب. Po.
- ج. Am.
- د. U.
8. العدد الذري لعنصر الروثينيوم هو 44، والعدد الكتلي له 101. ما عدد بروتونات هذا العنصر؟
- أ. 44.
- ب. 88.
- ج. 57.
- د. 101.
9. أي مما يأتي لا يمكن معرفة عمره باستخدام التأريخ الكربوني -14؟
- أ. وعاء خشبي.
- ب. شظايا العظم.
- ج. بقايا النبات.
- د. الأدوات الصخرية.
10. مم تتكون جميع المواد؟
- أ. الرمل.
- ب. ذرات.
- ج. أشعة الشمس.
- د. سبائك معدنية.
11. أي العبارات الآتية المتعلقة بالجدول الدوري صحيح؟
- أ. توجد العناصر جميعها بشكل طبيعي على الأرض.
- ب. تم ترتيب العناصر حسب زمن اكتشافها.
- ج. العناصر التي لها خصائص متشابهة تقع في المجموعة نفسها.
- د. رتبت العناصر حسب رأي مندليف.
12. أي مما يأتي لا يعد من خصائص الفلزات؟
- أ. قابلة للسحب والتشكيل.
- ب. لها لمعان.
- ج. قابلة للطرق.
- د. رديئة التوصيل للحرارة والكهرباء.
استخدم الرسم التالي للإجابة عن السؤالين 13 و 14.
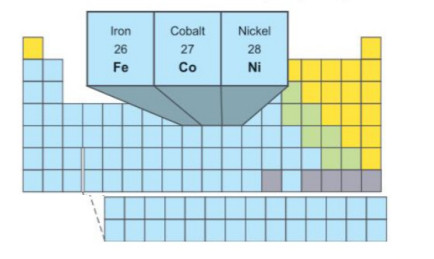
13. ما الاسم الذي يطلق على العناصر الثلاثة هذه التي تستخدم في عمليات صنع الفولاذ ومخاليط فلزات أخرى؟
- أ. اللانثانيدات.
- ب. الأكتنيدات.
- ج. الفلزات التي تصنع منها العملات.
- د. ثلاثية الحديد.
14. إلى أي مجموعة تنتمي العناصر البارزة في الجدول؟
- أ. اللافلزات.
- ب. الغازات النبيلة.
- ج. العناصر الانتقالية.
- د. الفلزات.
15. أي عناصر المجموعة 13 يدخل في صناعة علب المشروبات الغازية ونوافذ المنازل؟
- أ. الألومنيوم.
- ب. الإنديوم.
- ج. البورون.
- د. الجاليوم.
استخدم الجدول التالي للإجابة عن السؤالين 16 و 17.
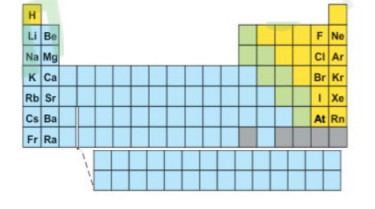
16. الهالوجينات عناصر لا فلزية نشطة. أي عناصر المجموعات الآتية يتحد معها بصورة سريعة؟
- أ. المجموعة 1 – الفلزات القلوية.
- ب. المجموعة 2 – الفلزات القلوية الأرضية.
- ج. المجموعة 17 – الهالوجينات.
- د. المجموعة 18 – الغازات النبيلة.
17. أي من الفلزات القلوية الآتية أكثر نشاطًا؟
- أ. Li
- ب. K
- ج. Na
- د. Cs
18. تُصنف الكثير من العناصر الأساسية للحياة – ومنها النيتروجين والأكسجين والكربون – ضمن مجموعة:
- أ. اللافلزات.
- ب. أشباه الفلزات.
- ج. الفلزات.
- د. الغازات النبيلة.
الجزء الثاني: أسئلة الإجابات القصيرة
س: ما العنصر؟
ج: العنصر مادة تتكون من ذرات تحتوي على العدد نفسه من البروتونات.
س: ما الاسم الحديث لأشعة الكاثود؟
ج: الإلكترونات.
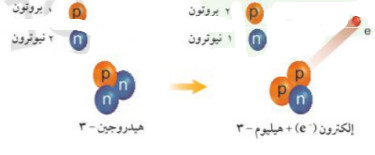
س: يوضّح الشكل أعلاه التحلل الاشعاعي (تحلل بيتا) للهيدروجين – 3 إلى هيليوم -3 وإلكترون، فما جسيم بيتا؟ ومن أي جزء من الذرة يأتي جسيم بيتا؟
ج: جسيم بيتا هو إلكترون ذو طاقة عالية يأتي من النواة وليس من السحابة الإلكترونية.
س: صف التحوّل الذي يحدث خلال تحلل جسيمات بيتا، كما هو موضح في الشكل أعلاه؟
ج: ينقسم النيوترون الذي في نواة الهيدروجين إلى إلكترون وبروتون يتحرر الإلكترون بكمية طاقة عالية ويبقى البروتون في النواة، فتتحول الذرة إلى الهيليوم.
س: وضح أفكار طومسون حول مكوّنات الذرة؟
ج: اعتقد طومسون أن الذرة كرة مصمتة ذات شحنة موجبة تنتشر الإلكترونات حولها بالتساوي.
س: هل تكون الإلكترونات بالقرب من النواة، أم بعيدًا عنها؟ ولماذا؟
ج: تكون الإلكترونات قريبة من النواة لأنها تنجذب إلى الشحنة الموجبة في النواة.
س: عمر النصف لعنصر السيزيوم -137 هو 30,3 سنة، فإذا بدأت بعينة كتلتها 60جم فكم يتبقى من العينة بعد 90,9 سنة؟
الإجابة:
عدد الفترات = 90.9 ÷ 30.3 = 3.
الكتلة المتبقية = 60 / 2³ = 7.5 جرام.
س: قارن بين خصائص عنصري الذهب والفضة اعتمادًا على معلومات الجدول الدوري؟
ج: كلاهما فلزات صلبة عند درجة حرارة الغرفة وينتميان إلى المجموعة 11. الفضة في الدورة الخامسة، أما الذهب فيوجد في الدورة السادسة.
س: لماذا لا يتطابق رمـــز العنصر أحيانًا مع اســــمـه؟ أعط مثالين على ذلك، وصف أصل كلّ رمز منهما؟
ج: تأتي تسمية العناصر في بعض الأحيان من الاسم اللاتيني، وقد تشمل الأمثلة الذهب Au الذي تأتي تسميته من الكلمة اللاتينية Aurum التي تعني العنصر اللامع. وكذلك الزئبق Hg الذي تأتي تسميته من الكلمة اللاتينية Hydrargyrum والتي تعني الفضة السائلة.
استخدم الرسم البياني التالي للإجابة عن السؤالين 28 و 29.
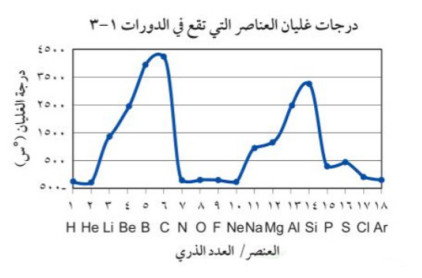
س: تظهر البيانات أن درجة الغليان خاصية دورية. وضّح المقصود بالخاصية الدورية.
ج: تظهر الخاصية الدورية نمطا معينا عندما تترتب العناصر حسب الزيادة في العدد الذري.
س: صف النمط الموجود في البيانات أعلاه؟
ج: تزداد درجات الغليان كلما اتجهنا من يسار الجدول الدوري إلى يمينه، حيث نجد أن مجموعة الكربون تعتلي قمة المنحنى، ثم تبدأ في بالانحدار مرة أخرى حتى تصل إلى مجموعة الغازات النبيلة.
س: صف الخليط الذي كان يستخدمه أطباء الأسنان قبل 150 سنة مضت لحشو الأسنان، ولماذا يستخدمون الآن مواد أخرى لحشو الأسنان؟
ج: يتكون الخليط من الفضة والنحاس والقصدير والزئبق. يعمل الأطباء حديثا على استخدام مواد أخرى لا تحتوي على الزئبق بسبب سميته العالية.
س: قارن بين الجدول الدوري الذي وضعه مندليف والجدول الدوري الذي وضعه موزلي.
ج: رتب مندليف العناصر في جدوله الدوري تبعًا للازدياد في الكتلة الذرية وكان هناك فراغات في جدوله لعناصر لم تكتشف حتى ذلك الحين. بينما رتب موزلي العناصر في الجدول الدوري تبعًا للعدد الذري، وكان هناك فراغات في جدوله أيضا، ولكن كان واضحًا عدد العناصر التي لم تكتشف بعد.
س: اختر مجموعة من العناصر الممثلة، واكتب قائمة بأسماء عناصرها، ثم اكتب 3 – 4 استخدامات لهذه العناصر؟
الإجابة:
مجموعة الكربون وتشمل: الكربون والسليكون والجيرمانيوم والقصدير والرصاص.
الاستخدامات:
- يستخدم الكربون في الماس و الجرافيت.
- يستخدم السليكون والجيرمانيوم كأشباه مواصلات.
- يستخدم القصدير في صناعة الأواني وطلاء العلب المعدنية.
- يستخدم الرصاص كمعطف واقي من الأشعة السينية.
الجزء الثالث: أسئلة الإجابات المفتوحة
استخدم الرسم التالي للإجابة عن السؤالين 34،33.
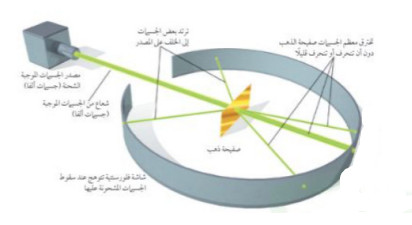
س: يوضح الرسم أعلاه تجربة راذرفورد. صف التجهيزات والإعدادات التي قام بها في التجربة، وما النتائج التي توقعها راذرفورد من تجربته؟
الإجابة:
تم إطلاق جسيمات ألفا على صفيحة رقيقة من الذهب محاطة بشاشة فلورسنتية تتوهج بالضوء عند سقوط جسيمات مشحونة عليها. توقع رادرفورد أن معظم جسيمات ألفا ستمر من خلال الصفيحة لتصطدم بالشاشة؛ لأنه كان يعتقد أن الصفيحة لا تحتوي على كمية كافية من المادة لإيقاف الجسيمات المشحونة أو تغيير مسارها، فقد اعتقد أن الشحنة الموجبة قد تحدث تغيرات يسيرة في مسار جسيمات ألفا.
س: ما دلالة ارتداد بعض الجسيمات من صفيحة الذهب؟ وكيف فسر راذرفورد هذه النتائج؟
ج: تظهر الجسيمات التي ارتدت عن مسارها بزوايا كبيرة أن نموذج طومسون للذرة غير صحيح. الشحنة الموجبة في الذهب تغير مسار الجسيمات، وقد اقترح رادرفورد أن معظم كتلة الذرة وجميع شحنتها الموجبة توجد في نواة الذرة.
س: صف أفكار دالتون حول مكوّنات المادة، والعلاقة بين الذرات والعناصر؟
ج: اعتقد دالتون أن المادة تتكون من ذرات وأن الذرات لا تنقسم إلى أجزاء أصغر منها، واعتقد أن ذرات العنصر الواحد متشابهة تماما، وأن العناصر المختلفة، تتكون من أنواع مختلفة من الذرات. وقد صوّر دالتون الذرة بأنها كرة صلبة مصمتة.
س: صف كيف اكتشفت أشعة الكاثود (المهبط)؟
الإجابة:
اكتشفت أشعة الكاثود التي نطلق عليها حاليًا اسم الإلكترونات في أواخر عام 1800م، اكتشفها العالم كروكس الذي استخدم أنبوبًا زجاجيًا مفرغا من الهواء، واستخدم قطعتين فلزيتين سماهما أنود (موجب) وكاثود (سالب)، موصولتان إلى البطارية بأسلاك ووضع في منتصفهما جسمًا مثبتًا في مسار الجسيمات، وعند توصيل البطارية يظهر ظل للجسم على الأنود موجب الشحنة، مما أثبت لكروكس أن الجسيمات تنتقل من القطب السالب إلى القطب الموجب.
س: صف كيف تمكن طومسون من توضيح أد أن أشعة الكاثود عبارة عن سيل من الجسيمات، وليست ضوءًا؟
ج: أعاد طومسون تجربة كروكس ولاحظ أن أشعة الكاثود تتحرك من القطب السالب إلى القطب الموجب ووضع طومسون مغناطيس بالقرب من أنبوبة كروكس فلاحظ انحناء الشعاع ولأن المغناطيس لا يؤدي إلى انحناء الضوء إذا فإن هذه الأشعة عبارة عن جسيمات مشحونة.
س: تحتوي بعض أجهزة كشف الدخان على مصادر مشعة. وضح كيف يستفاد من ظاهرة التحلل الإشعاعي في الكشف عن الدخان؟
ج: تحتوي أجهزة كشف الدخان على عنصر الأميرسون 241 الذي يمر بمرحلة التحول من خلال إطلاق الطاقة وجسيمات ألفا التي تسير بسرعة كبيرة جدا في الهواء فتتمكن من توصيل التيار الكهربي وعند اختراق الدخان للتيار الكهربي ينطلق جهاز الإنذار.
س: صف استخدامات العناصر المشعة في الطب والزراعة والصناعة؟
الإجابة:
- في الطب: تستخدم كمواد متتبعة لتشخيص الأمراض مثل اليود.
- في الزراعة: تستخدم كعناصر متتبعة لتتبع العناصر المغذية في النبات.
- في الصناعة: تستخدم لإنتاج أجهزة كاشف الدخان.
س: ما الدور المهم الذي يلعبه عنصر النيتروجين في جسم الإنسان؟ وضح أهمية البكتيريا للتربة التي تعمل على تحويل النيتروجين من حالته الطبيعية التي يوجد فيها؟
الإجابة:
يعتبر النيتروجين جزء من التركيب الخلوي الذي يحتوي على معلومات وراثية ويخزن الطاقة في جسم الإنسان.
تقوم البكتريا في التربة بتحويل النيتروجين إلى صورة يستطيع النبات امتصاصها فيحصل الإنسان على النيتروجين اللازم من خلال أكل النباتات.
س: يصنع العديد من الأسلاك المستخدمة في المنازل من النحاس. ما خصائص النحاس التي تجعله ملائما لهذا الغرض؟
ج: النحاس فلز وموصل جيد للكهرباء ذو درجة انصهار عالية يمكن ثنيه بسهولة كما يمكن سحبه على شكل أسلاك بسمك مختلف.
س: لماذا يقوم بعض أصحاب المنازل بالتحقق من وجود (أو عدم وجود) غاز الرادون النبيل في منازلهم؟
ج: الرادون غاز مشع ، يوجد في الصخور والتربة في بعض المواقع الجغرافية، وقد يتسرب إلى المنازل، وإطلاق الإشعاعات التي تسبب السرطان.
استخدم الرسم البياني التالي للإجابة عن السؤالين 44 و 45.
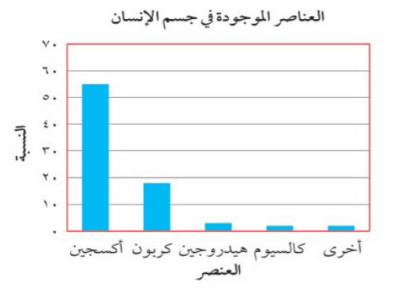
س: يوضح الرسم البياني أعلاه وجود بعض العناصر في الإنسان بكميات كبيرة. معتمدًا على المعلومات المعطاة في الجدول الدوري، صمّم جدولًا يوضّح خصائص كلّ عنصر على أن يتضمن رمزه وعدده الذري والمجموعة التي ينتمي إليها، وحدد ما إذا كان فلزًا أم لا فلز أم من أشباه الفلزات؟
الإجابة:
| العنصر | الرمز | العدد الذري | المجموعة | فلز / لا فلز |
| الأكسجين | O | 8 | 16 | لا فلز |
| الكربون | C | 6 | 14 | لا فلز |
| الهيدروجين | H | 1 | 1 | لا فلز |
| الكالسيوم | Ca | 20 | 2 | فلز |
س: أحد العناصر التي في الرسم أعلاه من الفلزات القلوية الأرضية. قارن بين خصائص عناصر هذه المجموعة وبين خصائص عناصر مجموعة القلويات؟
ج: الكالسيوم من العناصر القلوية الترابية ينتمي إلى المجموعة 2، وعناصر هذه المجموعة أكثر كثافة وأصلب وذات درجات انصهار أكبر من عناصر مجموعة الفلزات القلوية التي تقع في الدورة نفسها، وهي أقل نشاطا من الفلزات القلوية.