
بطاقة الدرس:
- عنوانه: الحرارة وتحولات المادة.
- ترتيبه: الثاني من الفصل الثالث «حالات المادة»، الوحدة الثانية «المادة والطاقة».
- مادة: العلوم.
- الصف: الثاني المتوسط.
- الفصل الدراسي: الأول.
- المدارس/المناهج: السعودية.
- الهدف: تلخيص/مراجعة وحل أسئلة.
- الدرس السابق: المادة
مقدمة: جسيمات المادة لها نوعين من الطاقة:
- طاقة الحركة.
- طاقة الوضع أو الكامنة.
تعريف الطاقة الحرارية: هي مجموع طاقة الوضع والطاقة الحركية لجميع جسيمات الجسم.
تعريف درجة الحرارة: هي متوسط الطاقة الحركية للجسيمات المكونة للجسم.
تعريف الحرارة: هي عملية انتقال الطاقة الحرارية من مادة درجة حرارتها أعلى إلى مادة درجة حرارتها أقل.
الحرارة النوعية
تعريفها: هي كمية الحرارة اللازمة لرفع درجة حرارة 1جم من مادة نقية درجة مئوية واحدة.
ملاحظات:
- كلما كانت الحرارة النوعية للمادة النقية عالية فهذا يعني أن المادة تبرد وتسخن ببطء.
- كلما كانت الحرارة النوعية للمادة النقية قليلة فهذا يعني أن المادة تبرد وتسخن بشكل أسرع.
- أعلى المواد حرارة نوعية هو الماء.
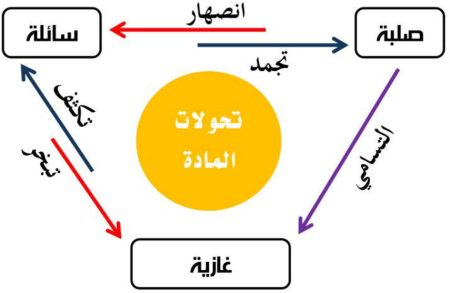
التغيرات بين حالات المادة
مقدمة:
- تتغير المادة من حالة إلى أخرى عند اكتسابها طاقة حرارية أو فقدانها طاقة حرارية ويعرف هذا التغيير بتغير الحالة.
- تكتسب المادة طاقة حرارية في الحالات التالية: (الانصهار – التبخر – التسامي).
- تفقد المادة طاقة حرارية في الحالات التالية: (التجمد – التكثف).
- المادة التي تكتسب طاقة حرارية تزداد الطاقة الحركية لجزيئاتها وكذلك تزداد طاقة الوضع لجزيئاتها.
- المادة التي تفقد طاقة حرارية تقل الطاقة الحركية لجزيئاتها وكذلك تقل طاقة الوضع لجزيئاتها.
التغيرات بين الحالات الصلبة والسائلة
الانصهار:
تعريفه: هو تحول المادة من الحالة الصلبة إلى الحالة السائلة.
ملاحظات:
- المادة تكتسب طاقة حرارية.
- تسمى درجة الحرارة التي يبدأ عندها التحول من الحالة الصلبة إلى السائلة بدرجة الانصهار وتساوي صفر مئوية.
- المركبات غير البلورية لا تمتلك تركيبا بلوريا لكي يتحطم وبالتالي فإنها لا تنصهر مثل المواد البلورية ولكنها تصبح أكثر ليونة.
التجمد:
تعريفه: هو تحول المادة من الحالة السائلة إلى الحالة الصلبة.
ملاحظات:
- المادة تفقد طاقة حرارية.
- تسمى درجة الحرارة التي يبدأ عندها التحول من الحالة السائلة إلى الصلبة بدرجة التجمد وتساوي صفر مئوية.
التغيرات بين الحالات السائلة والغازية
التبخر:
تعريفه: هو تحول المادة من الحالة السائلة إلى الحالة الغازية.
ملاحظات:
- المادة تكتسب طاقة حرارية.
- تسمى درجة الحرارة التي يبدأ عندها التحول من الحالة السائلة إلى الغازية بدرجة الغليان وتساوي 100 درجة مئوية.
أنواع التبخر:
- تبخر جميع جزيئات السائل (الغليان).
- تبخر جزيئات سطح السائل فقط.
التكثف:
تعريفه: هو تحول المادة من الحالة الغازية إلى الحالة السائلة.
ملاحظات: المادة تفقد طاقة حرارية.
التغيرات بين الحالات الصلبة والغازية
التسامي:
تعريفه: هو تحول المادة من الحالة الصلبة إلى الحالة الغازية مباشرة دون المرور بالحالة السائلة.
مثال: الجليد الجاف (ثاني أكسيد الكربون الصلب) – اليود – النفثالين.
ملاحظات: المادة تكتسب طاقة حرارية.
حل مراجعة الدرس
ج 1:
- الطاقة الحرارية: هي مجموع طاقة الوضع والحركة لجسيمات الجسم.
- درجة الحرارة: هي متوسط الطاقة الحركية لجسيمات الجسم.
ج 2: عندما تكتسب المادة طاقة حرارية تزداد الطاقة الحركية للجزيئات وتقل قوى التماسك بين الجزيئات والعكس فعندما تفقد المادة طاقة حرارية تقل الطاقة الحركية للجزيئات وتزداد قوى التماسك بين الجزيئات.
الأمثلة:
- انصهار الجليد.
- غليان الماء.
ج 3: حالة الانصهار – حالة التبخر – حالة التسامي.
ج 4:
- تبخر لجميع جزيئات السائل.
- تبخر لسطح السائل فقط.
ج 5: السبب لان الماء الموجود على الجلد يمتص الحرارة من الجسم ويتبخر فتشعر بالبرودة والقشعريرة
ج 6: درجة الحرارة ثابتة لأن الطاقة الحرارية الممتصة تستخدم في تحطيم وتكسير الروابط (قوى التماسك) بين الجزيئات.
ج 7: متروك للمعلم (يجب أن تكون الإجابات قريبة من 69.5 درجة مئوية).
ج 8:
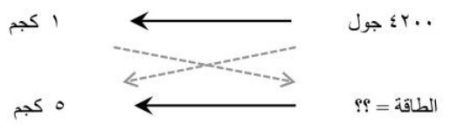
الطاقة = 4200 × 5 × 10 = 210000 جول.
⇐ درس مُقترح للمراجعة: المحاليل الحمضية والمحاليل القاعدية